真核生物基因組極具復雜性。如何將宏觀尺寸的基因組DNA包裝入微米級的細胞核中是生命科學的基本問題之一。在細胞周期中,基因組具有高度組織性。在細胞周期間期,基因組形成不同的區室(Compartment)和結構域(Domain),而在有絲分裂期,基因組被高度凝聚成X形染色體。一類高度保守的ATP酶多亞基蛋白質復合物——SMC復合物,在基因組的三維結構中扮演中關鍵的角色【1-3】。真核生物的SMC復合物包括粘連蛋白(Cohesin),凝縮蛋白(Condensin)以及SMC5/6復合物。粘連蛋白的主要功能是介導間期染色質環結構域(Loop domain)和拓撲相關結構域(Topologically associating domain,TAD)的形成以及細胞分裂中姐妹染色單體的粘連。凝縮蛋白介導有絲分裂中的染色體凝聚。粘連蛋白和凝縮蛋白一起保證了有絲分裂末期姐妹染色單體的正常分離。雖然SMC復合物對細胞活動至關重要,然而其作用機制仍不清楚。
人類粘連蛋白由SMC1,SMC3,RAD21以及STAG1/2四個亞基組成,并且能夠形成環狀結構。在裝載蛋白NIPBL-MAU2的幫助下,粘連蛋白加載到染色體上發揮功能【4,5】。NIPBL的突變會引起發育相關疾病包括德朗熱綜合征(Cornelia de Lange syndrome)的發生。大量證據表明粘連蛋白與CTCF一起調控有絲分裂間期基因組組織和基因轉錄,并提出粘連蛋白通過環擠壓(Loop extrusion)方式來介導染色質結構域的形成【6,7】。2018年初,研究人員在體外觀測到酵母凝縮蛋白介導的DNA環擠壓過程【8】。然而對于粘連蛋白是否具有該活性,仍缺乏直接的證據。
2019年11月29日,來自美國得克薩斯大學西南醫學中心于洪濤教授課題組與得克薩斯大學奧斯汀分校的Ilya J. Finkelstein教授課題組合作,在Science上在線發表題為Human cohesin compacts DNA by loop extrusion的研究論文(Yoori Kim博士和史竹兵博士為共同第一作者,Hongshan Zhang博士為共同作者),他們利用單分子成像技術在體外實時觀測到重組的人源粘連蛋白-NIPBL復合物可以壓縮裸露的以及核小體結合的DNA,并證明粘連蛋白-NIPBL復合物通過ATP驅動的環擠壓方式來壓縮DNA。值得一提的是,來自奧地利的Jan-Michael Peters課題組近期也有類似的發現【9】。另據悉,于洪濤教授會于2019年12月份全職回國工作,在西湖大學組建實驗室。

在于洪濤課題組的研究中,研究人員首先克服了人源粘連蛋白以及粘連蛋白-NIPBL復合物表達與純化的困難,獲得高質量的蛋白樣品用于單分子成像研究。體外酶活實驗發現,粘連蛋白本身具有非常低的ATP酶活性,而NIPBL和DNA可以顯著提高其ATP酶活性。負染電鏡結果顯示粘連蛋白-NIPBL復合物具有多種構象,可能代表ATP水解以及DNA結合時的不同狀態。
令人振奮的是,研究人員利用全內反射熒光顯微鏡,實時觀測到粘連蛋白-NIPBL復合物可以作為分子馬達壓縮固定于脂雙層表面的線形DNA。在未加粘連蛋白-NIPBL復合物時,這些線性DNA通過溶液流動得到完全伸展。粘連蛋白-NIPBL復合物非常有效地以0.5 kb/s的平均速率壓縮DNA,并且這一過程依賴于ATP水解,而單獨的粘連蛋白不具有DNA壓縮功能。通過改變溶液流速進而改變DNA所受應力,研究人員發現應力的增加導致DNA壓縮速率的降低,說明粘連蛋白-NIPBL復合物介導的DNA壓縮是力敏感的。更為重要的是,人們一直認為粘連蛋白通過拓撲結合方式將DNA捕獲在環狀結構里來發揮功能,然而研究人員發現高濃度鹽緩沖液可以逆轉DNA壓縮過程,暗示粘連蛋白是以非拓撲DNA結合方式來壓縮DNA的。為了模擬體內的染色質狀態,研究人員在上述實驗的基礎上引入核小體。結果顯示,與裸露DNA相似,粘連蛋白-NIPBL復合物以相同的速率壓縮核小體結合的DNA。這一過程同樣依賴于ATP水解,而且也是力敏感的。這些結果表明,在細胞內,核小體的存在不影響粘連蛋白引發的染色質壓縮(圖一)。
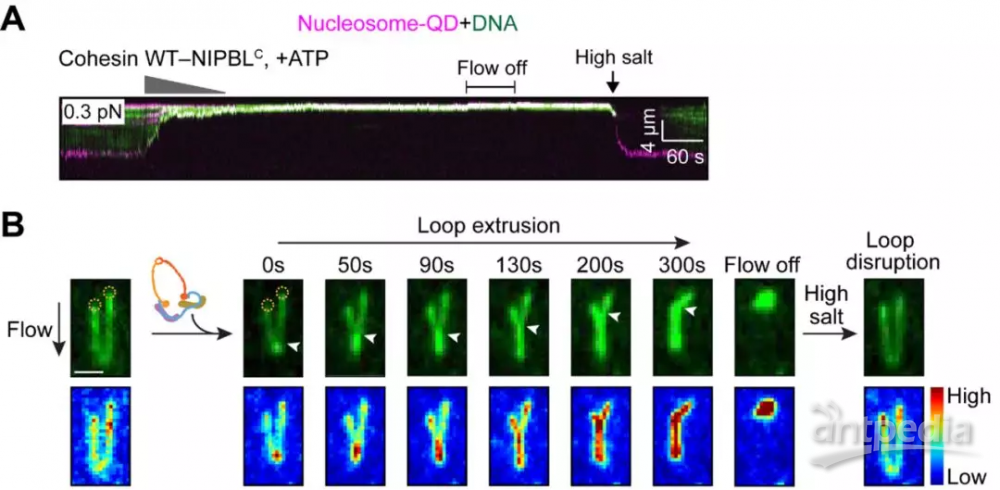
圖一
進一步地,研究人員制備了兩端錨定的“U”型DNA分子來直接觀察DNA環擠壓過程。當將粘連蛋白-NIPBL復合物注入“U”型DNA中,DNA環開始從其頂部開始伸出,直至DNA的一側錨定點(圖一)。值得注意的是,之前的研究顯示凝縮蛋白以不對稱的方式來進行DNA壓縮,然而于洪濤課題組的研究發現粘連蛋白-NIPBL復合物以對稱的方式從“U”型DNA兩側同時壓縮DNA。粘連蛋白-NIPBL復合物介導的DNA環擠壓過程以0.5 kb/s的平均速率持續作用到數萬堿基對上,并且最大速率可達到1.3 kb/s。通過熒光標記粘連蛋白并利用光漂白實驗發現,粘連蛋白-NIPBL復合物與DNA環基部共定位,并在多數情況下粘連蛋白-NIPBL復合物以二聚體的形式發揮功能(圖二)。這與已報道的凝縮蛋白亦不相同。凝縮蛋白以單體的形式單方向不對稱地壓縮DNA,而粘連蛋白以二聚體的形式雙向對稱地介導DNA環擠壓過程。因此,雖然SMC復合物具有相似的結構,然而具體的作用機制截然不同。在原核生物中,僅有一種SMC復合物存在。體內的證據顯示原核SMC復合物也可能是以二聚體形式發揮DNA壓縮功能。因此,在進化過程中,生命體生成不同的SMC復合物,它們在特定的時期以不同的方式行使相似但特異的生物學功能。

圖二
綜上,這項研究為粘連蛋白環擠壓模型提供了直接的實驗證據。粘連蛋白-NIPBL復合物作為ATP水解驅動的分子機器,以二聚體作為基本功能單元,非拓撲形式結合并雙向壓縮DNA,形成對稱的DNA環結構域。這一結果與已報道的高通量染色體構象捕獲技術(Hi-C)數據,細胞內相關研究以及理論模擬模型相吻合。考慮到粘連蛋白的重要生物學功能,這項研究為進一步深入理解真核基因組結構和基因轉錄調控機制奠定了基礎,也為相關疾病發生機理的闡明提供了理論依據。
原文鏈接
https://science.sciencemag.org/content/early/2019/11/25/science.aaz4475
制版人:小嫻子
參考文獻
1. Jeppsson, K., et al., The maintenance of chromosome structure:positioning and functioning of SMC complexes. Nat Rev Mol Cell Biol, 2014. 15(9): p. 601-14.
2. Rowley, M.J. and V.G. Corces, Organizational principles of 3D genomearchitecture. Nat Rev Genet, 2018. 19(12):p. 789-800.
3. Uhlmann, F., SMC complexes: from DNA to chromosomes. Nat Rev Mol Cell Biol,2016. 17(7): p. 399-412.
4. Ouyang, Z. and H. Yu, Releasing the cohesin ring: A rigid scaffoldmodel for opening the DNA exit gate by Pds5 and Wapl. Bioessays, 2017. 39(4).
5. Zheng, G. and H. Yu, Regulation of sister chromatid cohesionduring the mitotic cell cycle. Sci China Life Sci, 2015. 58(11): p. 1089-98.
6. Nasmyth, K. and C.H. Haering, Cohesin: its roles and mechanisms. AnnuRev Genet, 2009. 43: p. 525-58.
7. Alipour, E. and J.F. Marko, Self-organization of domain structures byDNA-loop-extruding enzymes. Nucleic Acids Res, 2012. 40(22): p. 11202-12.
8. Ganji, M., et al., Real-time imaging of DNA loop extrusion bycondensin. Science, 2018. 360(6384):p. 102-105.
9. Davidson, I.F., et al., DNA loop extrusion by human cohesin.Science, 2019.
三維基因組互作與表觀遺傳修飾是基因表達調控的重要因素,其動態變化與細胞生長發育及癌癥等疾病的發生發展密切相關。解析染色質在活細胞內的時空動態,是理解基因調控機制的重要科學問題。現有基于CRISPR-C......
1812年,法國皇帝拿破侖一世從俄羅斯莫斯科撤退時,其大部分軍隊因饑餓、疾病和寒冷的冬天而損失殆盡。如今,對這撤退途中喪生的30萬士兵的部分遺骸的DNA的分析發現,兩種未曾預料到的細菌性疾病很可能增加......
1812年夏,法蘭西皇帝拿破侖·波拿巴率50萬大軍入侵俄羅斯帝國。然而到12月時,這支軍隊僅余零星殘部。歷史記載將此次“全軍覆沒”歸因于饑寒交迫與斑疹傷寒。但一項新研究表示,從士兵牙齒中提取的DNA,......
美國北卡羅來納大學研究團隊研發出一種名為“DNA花朵”的微型機器人。這種機器人具有獨特的自適應環境變化能力,能夠像生物體一樣,根據周圍環境改變形狀和行為。“DNA花朵”機器人由DNA與無機材料結合形成......
瑞士蘇黎世聯邦理工學院科學家在最新一期《自然》雜志上發表論文稱,他們開發出一款名為MetaGraph的DNA搜索引擎,能快速、高效地檢索公共生物學數據庫中的海量信息,為研究生命科學提供了強大的專業工具......
究竟是什么讓人腦與眾不同?美國加州大學圣迭戈分校研究團隊發現了一個名為HAR123的小型DNA片段,這將是解開人類大腦獨特性之謎的關鍵。相關研究成果發表于新一期《科學進展》雜志。最新研究表明,HAR1......
究竟是什么讓人腦與眾不同?美國加州大學圣迭戈分校研究團隊發現了一個名為HAR123的小型DNA片段,這將是解開人類大腦獨特性之謎的關鍵。相關研究成果發表于新一期《科學進展》雜志。最新研究表明,HAR1......
基因組編輯技術作為生命科學領域的一項重要突破,為基礎研究和應用開發提供了技術支撐。以CRISPR及其衍生技術為代表的編輯系統通過可編程的向導RNA引導Cas9等核酸酶靶向基因組特定位點,被廣泛應用于特......
神經元中基因編輯的插圖。圖片來源:杰克遜實驗室哪怕在五年前,人們也會認為在活體大腦中進行DNA修復是科幻小說中才有的情節。但現在,科學家已能進入大腦、修復突變,并讓細胞在整個生命周期中維持住這種修復效......
國際知名學術期刊《自然》北京時間7月2日夜間在線發表一篇基因組學論文稱,研究人員從上埃及Nuwayrat地區一個古王國墓葬中提取到一名古埃及個體的全基因組測序數據,這些數據分析可追溯至古埃及第三至第四......