在研項目:中樞神經系統疾病(阿爾茨海默癥和帕金森病)藥物研發包括靶點化藥以及上市化學藥和中藥的二次開發。
續上文。
2.治療
治療藥物方面,早發現早治療AD目前被大多數人接受為最有可能有效幫助的AD病人的策略。隨著Aβ PET顯像示蹤劑美國藥監局批準上市和Tau PET顯像示蹤劑的批準臨床研究,大藥企開始使用這兩個生物標志物篩選病人入組或者作為療效測試指標。
2.1 膽堿能系統
膽堿酯酶是AD藥物研發最為成功的靶點,美國藥監局目前為止只批準了5個AD新藥(NCE),其中4個是膽堿酯酶抑制劑(表一)。這個領域目前在研新產品不多,可以查到進行中臨床試驗只有2個;一個1期臨床藥物以及一個石衫堿甲的4期臨床試驗。
2.1.1 VU0467319
范德堡大學研發的毒蕈堿型乙酰膽堿受體(mAchR1)正向別構調節劑(positive allosteric modulator),即PAM激動劑,預計今年上半年開始一期臨床(2)。這個靶點一度很受重視,但因傳統激動劑對外周系統的毒副作用和Aβ假說的重視影響了這個靶點的進程。
2.1.2 石衫堿甲
上海市精神衛生中心2016年11月開始做的石衫堿甲的4期臨床試驗,在300個MCI期AD病人中做為期52周的MCI到AD轉化率的實驗,預計2018年12月完成(2017年12月完成數據采集)。
2.2 淀粉樣蛋白病變
這個機制目前在研的藥物最多,也出現了許多失敗的情況。在研藥物包括小分子,抗體和疫苗。目前,2/3和3期臨床試驗的藥物預計2019年開始會有結果,這個假說是否可以影響AD病情在2020-2023年之間估計可以得出定論。如果安全并可以降低Aβ斑塊(而且伴有一定認知效果),這方面的藥物將可能被FDA批準,跟降膽固醇的藥預防心臟病一樣,在Aβ異常增高的人群中使用。
2.2.1 小分子藥物
針對淀粉樣蛋白病變假說的小分子靶點主要是Aβ預蛋白APP代謝通道的三個內泌酶(secretase):α, β和γ內泌酶。其中研究最多的是β內泌酶,BACE。另外有許多靶點可以間接的影響淀粉樣蛋白病變。
α-內泌酶是個很好的靶點,需要激活劑,雖然目前酶激活劑本身的研發還沒有太好辦法,但可以通過信號通路激活。比如上面提到的毒蕈堿型乙酰膽堿受體激動劑的可以 通過調節蛋白K激酶(PKC)活性來增加α-內泌酶活性。另外從苔鮮動物草苔蟲(Bugula neritina)中提取出的一種大環內酯類物質Bryostatin 1(苔蘚蟲素)也被發現有PKC調節作用,并對1例嚴重家族性AD病人有效果,目前Neurotrope正在進行2期臨床試驗。同時Aphios公司也在進行Bryostatin衍生物的研究,APH-0703在巴哈馬做了一例AD病人,,公司網站稱結果“顯著、鼓舞人心”,目前該公司正在研發比APH-0703活性更好的在預臨床階段的衍生物APH-104。
γ-內泌酶一度有很多公司在研發,但底物非特異抑制劑臨床證明抑制γ-內泌酶不但不能幫助AD病人反而可以加重病情(5),公認的原因是γ-內泌酶有好多APP以外的底物如Wnt, 抑制這些底物的活性導致毒副作用。目前選擇性γ-內泌酶調節劑的研究在進行中,輝瑞的PF-06648671已經進入臨床期。
2.2.1.1 BACE抑制劑
目前在研的2-3期臨床的BACE抑制劑共有6個藥物,上面提到的楊森的JNJ-54861911和諾華/安進的CNP520在做預防性試驗(1.5,1.6)。其他4個見表二,其中兩個獲得美國藥監局的綠色通道身份(Fast Track designation)。這個靶點是否有效2019年底2020年初可以知道初步結果。不過默沙東剛宣布的Verubecestat的3期臨床失敗(表二,紅顏色),為這個靶點帶來嚴重危機,但禮來/阿斯利康今年3月開始1400病人的現在進行實驗的延續(表二,綠顏色),也表明了這兩家大藥企對BACE靶點的信心!
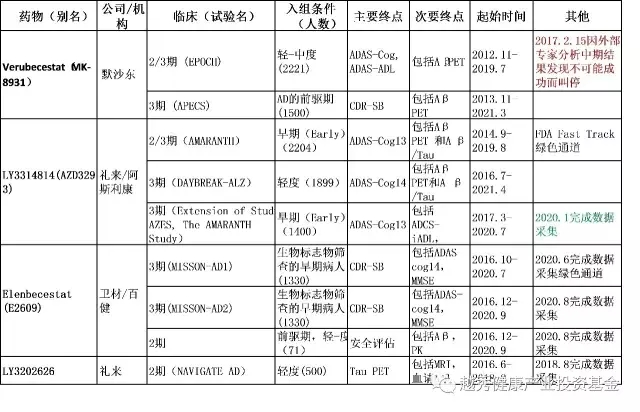
表二:2-3期在研BACE抑制劑(數據來源:clinicaltrials.gov; yahoo.com搜索和Eisai.com)
2.2.1.2 其他影響Aβ的在研小分子藥物
文獻中的可以通過不同途徑影響或清除Aβ的小分子有很多。除了上面提到的輝瑞的γ-內泌酶調節劑,下面是4個不同機制的在研的其他影響Aβ的小分子藥物,最早的2018年可以知道結果。
2.2.1.2.1 Azeliragon (TTP488, PF-04494700)
RAGE受體抑制劑,抗氧化并有清除Aβ作用。vTv 藥物公司2013年獲得FDA綠色通道,2015年4月開始在800個輕度AD病人中做一個叫STEADFAST的3期臨床,預計2019年1月完成。
2.2.1.2.2 ALZT-OP1(色甘酸鼻噴劑Cromolyn和布洛芬Ibuprofen)
老藥新用聯合新用,布洛芬抗炎癥,色甘酸有抗Aβ聚集和降低Aβ作用。 AZTherapies公司2015年9月開始在600個早期病人中做一個叫COGNITE的3期臨床,預計2018年3月完成。
2.2.1.2.3 CT1812
Sigma-2/PGRMC1受體結合劑,可以抑制Aβ與Sigma-2/PGRMC1受體結合。CogRx公司2015年9月開始在114個健康志愿者進行1期臨床,2016年5月完成。2016年9月1/2期臨床開始在16個早中期AD病人在澳大利亞的幾個中心進行。
2.2.1.2.4 PF-05251749
沒有透露具體機制的第二個1期檢測腦脊液Aβ。輝瑞2016年11月公司產品鏈列舉此化合物為AD在研產品,已完成1個一期臨床。并在2016年6月在比利時54個健康和健康老人中開始第二個一期臨床。
2.2.2 抗體藥物
針對Aβ的抗體是這個領域做的最多的,也是失敗最多的。在五個臨床數據最多的Aβ抗體中,輝瑞的Ponezumab和輝瑞/楊森的Bapineuzumab已經被放棄,但羅氏/基因泰克的Crenezumab (MABT510A)(1.3,表三),羅氏/基因泰克/中外制藥的Gantenerumab (RG1450)(1.1,表三)和禮來的Solanezumab(1.1,1.4)都獲得了新生。雖然禮來的新總裁剛剛宣布終止了剛開始的SolanezumabExpediton PRO3期臨床試驗(6, 表三紅顏色)但羅氏剛宣布開展一個新的Crenezumab3期臨床試驗(表三,綠顏色)。目前業內最看好的是百健的Aducanumab (BIIB 037,表三)。盡管2016年公布的Aducanumab的1期臨床數據揭示能夠有效減緩早期AD病人的認知功能減退,但如何控制副作用和進行中的2個3期臨床是否能重復這個樣本很小但到目前為止Aβ領域最好的結果只有時間可以回答。希望2020年可以有好消息。
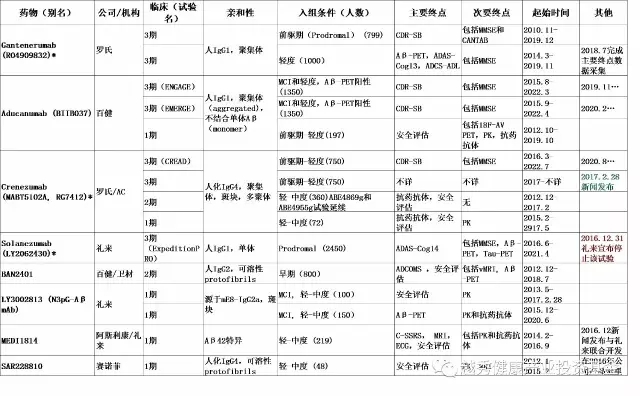
表三:在研Aβ抗體藥物
2.2.3 疫苗
疫苗是個非常有前景的方向,但包括腦膜腦炎在內的毒副作用是個亟待解決的難點。目前Aβ領域至少有6個臨床期疫苗。
2.2.3.1
諾華的CAD106疫苗在做2/3期預防臨床試驗(1.6)走在最前沿。
2.2.3.2
AC Immune公司的ACI-24疫苗在做兩個臨床試驗:2009年開始在歐洲不超過198個AD病人中進行 1/2期臨床試驗,何時完成不詳和2016年3月開始在美國24個唐氏綜合癥病人中進行1期臨床,預計2019年8月完成。
2.2.3.3
Araclon的ABvac 40和ABvac42疫苗沒有在世界衛生組織或Clinicaltrials.gov上登錄,但公司網站顯示已在2015年分別進入1期和2期臨床。
2.2.3.4
AFFiRiS公司2010年9月到2013年2月在歐洲做了332個AD病人的AFFITOPE AD02疫苗2期臨床試驗,結果發現疫苗沒有效果。但有意思的是輔助免疫配方(后來被該公司命名為AD04)對照組(~50病人)有約一半病人的病情得到緩解。AFFiRiS公司還在思考下一步如何進行。
2.4.5
United神經科學公司的UB-311疫苗2015年10月開始在臺灣的45個輕度病人中進行2期臨床試驗,預計2017年12月完成。
2.4.6
靈北2015年3月開始在35個輕度病人中開始Lu AF20513疫苗的1期臨床試驗,預計2017年5月完成。
2.3 Tau蛋白病變
針對Tau蛋白病變的在研藥物不多,可以查到的臨床研發藥物有6個:2個小分子,2個抗體和2個疫苗。
2.3.1小分子藥物
2.3.1.1 LMTM,亞甲藍(Methylene blue)衍生物
前面提到TauRx公司2016年宣布LMTM 的第二個3期臨床失敗,但TauRX聲稱LMTM在完成的兩個3期臨床試驗中LMTM單獨使用組跟LMTM與Aricept聯合用藥組對照有明顯療效,雖然在測試過的劑量中沒有量效關系。TauRx公司的這個分析方式遭到很多非議因為單獨用藥組沒有相應安慰劑對照組,但公司準備繼續LMTM的研發,正在籌備LMTM單獨用藥臨床試驗。
2.3.1.2 TPI 287
Cortice公司的可以影響Tau病變的的抗癌藥。加州大學舊金山分校2013年11月開始在33個輕到中度病人中進行1期臨床,預計2017年11月完成。
2.3.2 抗體藥物
2.3.2.1 ABBV-8E12(C2N 8E12)
AbbVie公司2015年3月從C2N公司轉讓而來的Tau抗體,2016年10月開始在400個早期AD病人中進行2期臨床,預計2020年4月完成。公司聲稱可以盡快在不同的適當時機知道試驗結果,最大程度推進研發速度。
2.3.2.2 RO 7105705(RG 6100)
基因泰克和AC Immune公司聯合開發的Tau抗體。基因泰克2016年6月開始在71個健康人和輕度到中度AD病人中進行1期臨床試驗,預計2017年5月完成。
2.3.3疫苗
2.3.3.1
AADvac-1是Axon 神經科學公司針對Tau氨基酸294到305的疫苗,2016年3月開始在185個輕度AD病人中進行2期臨床試驗,預計2019年2月完成。
2.3.3.2
ACI-35是AC Immune公司研發的針對磷酸化Tau蛋白的疫苗,2013年12月開始在24個輕度到中度的AD病人中開始1期臨床試驗, 2015年轉讓給強森公司,目前進展不詳。