開發異源蛋白制備工藝,需要進行大量的平行培養試驗,大多是在震動瓶中或者微孔板上來進行批次培養。所面臨的重要挑戰則是如何對培養條件進行控制。為達此目的我們采用了現代化傳感技術以及統計學的實驗設計—DoE最佳實驗設計。
在生物工程領域,小到毫升級別,大到工業生產規模級別,為縮短生產過程的開發時間,進行實用的方法開發是其前提條件。本文的研究中,采用了統計學的實驗設計(DoE),按照兩種不同的培養規模微升級和毫升級,求出最佳培養參數。
通常分批培養法都是在震動體系(主要是震動瓶,也包括微孔板和臺式發酵儀)中進行的,旨在以較小的耗費來獲得實驗結果。可惜這里并未考慮到生產規模的條件及其對于產品的收率和質量的影響。
究其原因就是:
培養是分批次進行的,工業化的生物過程在原則上也屬于一種基底限制的補料分批培養過程,其碳料的加入和其pH值的演變也受到控制。
培養中沒有考慮濃度梯度的影響,尤其是在大比例的放大過程中,由于攪拌裝置效率受限而可能引起的濃度梯度。
在實驗室規模的批次培養中,碳源在起始階段呈現為高濃度,許多細菌的數量是以指數的方式生長形成有機酸,致使pH值隨時間發生變化。對于溶解氧而言,可能在震動瓶局部形成梯度。此外,在震動瓶中進行的培養沒有明顯出現介質組成的濃度梯度。微孔板如同震動瓶一樣具有局限性,所得到的附加信息很少的,這是因為對于這樣小體積的取樣和精確分析是很有限的。
非常重要的一點就是,對于每種培養規模(微孔板、瓶、微反應器、工業化規模的大反應器)
而言,都要能夠知道其結果所具有的說服力邊界是什么。
此外開發可靠的數學計算和分析方法以及監視和控制的方法也很有意義,以便獲得不同發展階段中較為準確的信息。
本文進行了補料分批培養法按照兩種不同規模:采用24式微孔平臺(3.3ml)和震動瓶(125ml)分別進行培養比較。運用了presens precising sensing有限公司的傳感器技術,能夠對兩種培養規模的pH值和溶解氧(DO)進行監測(見圖1)。依此建立起微升和毫升級規模間的數學關系,以微孔板培養中所獲得的數據為基礎,按照此前所確定的最佳實驗條件,移植到震動瓶或發酵儀中再進行后續試驗。此舉目的在于利用小規模的培養同時獲取更多附加信息。這樣一來,可以降低之后的任何放大尺寸規模的試驗次數。
材料與方法
為了在微孔板上和震動瓶中進行這種基底限制的補料分批培養試驗,采用了Anbase系統(Biosilta公司)。此系統是從溶解的聚合物中將葡萄糖通過生物催化釋放出來。培養過程中葡萄糖的攝入量是通過加入催化劑的量測得,微孔平臺或是震動瓶中培養時達到最大生長點時,釋放葡萄糖所需的生物催化劑其最佳體積和理想濃度值就是以上試驗的測定目的。
借助軟件Modde 9.1(Umtrics)確立采用的參數值:生物催化劑的濃度(0-30 U/L)和體積(在24孔板中為0.5~2.1ml,在震動瓶中為7~15ml);最佳密度為波長600nm時測得。取不同體積和催化劑濃度以不同的規模共進行了11次試驗。這種24孔氧盤(Oxodish)和水盤(Hydrodish) 配備有SDR傳感器測量系統(Presens公司)。而震動瓶(總體積125ml)則配備有通過SFR Shake Flask 讀出裝置的pH值、溶解氧值監測傳感器。傳感器盤和孔板是通過特殊的蓋子和鉗具的結合來獲得氧氣。
此外為了對兩種規模的pH值、溶解氧進行在線測量,對于細菌的生長采用了分光光度法于600納米波長進行測量(OD600)。憑借這種補料分培養法,成功實現了大腸桿菌BL21在Enpresso B 介質中的培養(Biosilta)。這種培養的起始光密度OD600介于0.1 – 0.3之間。在培養的全程時段中,其pH值和溶解氧值的飽和度不僅能夠在微孔板中而且也在震動瓶中受到連續監測,借以評估養條件,進而保證細菌的培養得以在pH 7 – 7.5之間和不會出現氧氣限制的條件下生長。為此要在規律的時間間隔將樣品取出進行光度法測量。
微孔板對照震動瓶
正如從圖2中所見,所有溶解氧的進程對于基底限制的補料分批培養法而言均是特征性的。在每項試驗中,生物催化劑的活性大致上都是保持一致的。這樣反過來又導致葡萄糖的供給對于整個培養過程也都是大致相同的。在第一階段,由于低的細胞密度,限制了葡萄糖的吸收,導致葡萄糖的富集和細菌首次的指數式的生長階段。這也如多數工業化生產所期待的那樣。細菌呼吸頻率的強烈增加并伴以指數式的生物聚集體的增長,可以明顯地體現于溶解氧(DO)曲線的加速下降中。pH-值的下降,表明了細菌排泄產生了有機酸,主要為乙酸。第二階段則是以基底限制為特征的。過剩的葡萄糖已被耗盡,細胞的生長和呼吸的速率,對于每一培養方法而已,都是通過葡萄糖的釋放速率加以測得的。葡萄糖濃度的開始下降,不僅是在SDR抑或SFR體系中,對于每一種培養而言,均是與釋放葡萄糖的生物催化劑的量有關的。通過對葡萄糖加入劑量的優化,可以調節葡萄糖釋放的速率,使之在培養過程中不至于出現厭氧階段(見圖2 A-C)。如同所期待的那樣,氧的轉移在震動瓶中要比在微孔板系統中進行得更好,所以能夠將震動瓶中催化霉的濃度從4提高到23U/L,而并不出現缺氧的情況。在微孔板的SDR系統中出現的趨勢,可以在震動瓶的SDR-系統中加以重現。相似的情況還出現于兩種培養系統中的溶解氧和pH-的曲線廓形(見圖2 D-F),證實了培養的重現性。介于不同凹穴和不同培養之間的差異,從統計學上看,沒有什么意義(數據未予展示)。

圖1.于一震動器上所結合的Shake-Flsk讀數器和傳感器盤讀數器。
總結
氧和pH-的測量,對于生物生產的培養過程中生理狀態的監控是不可或缺的。如果能夠提供一種可能性,將溶解氧的飽和度和pH-值在采用微孔板和震動瓶中掃描試驗的培養過程的早期就予以監測,這對于較快地進行生物過程開發而言,當是一種重要的貢獻。將這種測量系統結合于適合的控制方略和基于先進模式的試驗設計,則能夠通過少量的試驗,以微小的人力和物力的耗費,取得進行有效的擴大試驗所需要的基礎性數據。如果細胞培養能夠在有氧的、基底限制的和pH-穩定的條件下進行的話,那么這種小規模試驗與大規模生產之間的相關性就會增加。實驗室規模有控制的補料分批培養法,不僅能夠獲得較高的細胞密度和產率,而且還能得到大規模生產條件的較大近似性。結合基底脈沖技術,在本文的研究中業已能夠將工業規模的異質條件復制出來,使得細胞培養免于不斷交替地處于基底不足或者基底過剩的區域。
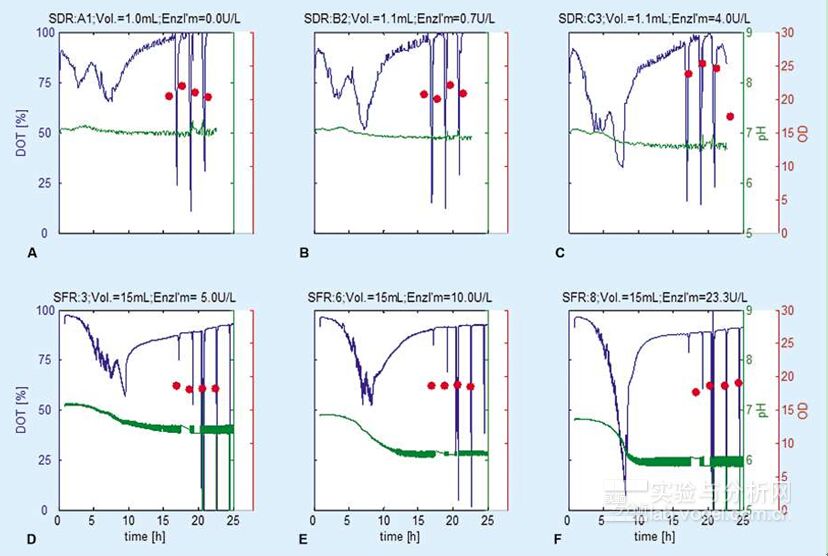
圖2.大腸桿菌BL21培養過程的在線監測:(A-C) 在微孔板中pH值和溶解氧的測量;(D-F) 在震動瓶中pH值和溶解氧的測量。
更加快捷的生物過程開發
如果能夠提供一種可能性,將溶解氧的飽和度和pH-值在采用微孔板和震動瓶中掃描試驗的培養過程的早期就予以監測,這對于較快地進行生物過程開發而言,當是一種重要的貢獻。將這種測量系統結合于適合的控制方略和基于先進模式的試驗設計,則能夠通過少量的試驗,以微小的人力和物力的耗費,取得進行有效的擴大試驗所需要的基礎性數據。