為了解釋別構酶協同效應的機制并推導出動力學曲線的方程式,不少人曾提出過各種模式,各有優缺點,現在主要把Hill模式敘述如下:
Hill模式
在協同結合模式中最早的一種是Hill在1909年提出的,企圖解釋氧結合至血紅蛋白的S形飽和曲線,現稱為Hill模式,后來經Atkinson應用于別構酶反應,他設想在這個系統中,n分子的配體(S)能夠一步結合到酶上去:
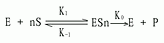
即此反應的總解離常數(K's)由下式決定
K'S=[E][S]n/[ESS] | (6-7) |
而酶的飽和分數
YS=每分子酶蛋白上已結合的底物分子數/每分子酶蛋白上底物結合位點的總數 | (6-8) |
又因總的酶濃度[E0]=[E]+[ES0]
故 YS=[ESn]/[E0]=[ESn]/[ESn]+[E] | (6-9) |
合并式6-7和式6-9,消去[ESn],則
YS=[S]n/K'S+[S]n | (6-10) | ||
YSK'S+YS[S]n=[S]n, | |||
YSK'S=(1-Y)[S]n | (6-11) | ||
Ys/1-Ys=[S]n/K'S | (6-11) | ||
| log | [YS/(1-YS)] | =nlog[S]-logK'S | (6-13) |
因此以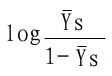 對log[S]作圖的話,可得斜率為n,縱軸截距為-logK'S的直線(見下圖)。
對log[S]作圖的話,可得斜率為n,縱軸截距為-logK'S的直線(見下圖)。
因v=k0[ESu],Vm=k0[E0],故
| (6-14) |
將式6-10代入式6-14,即得
[S]n/K'S+[S]n=v/Vm | |
Vm[S]n=K'Sv+v[S]n | (6-15) |
(Vm-v)[S]n=K'Sv | (6-16) |
v/Vm-v=[S]n/K'S | (6-17) |
logv/Vm-v=nlog[S]-logK'S | (6-18) |
式6-13或6-18即為Hill方程式,式6-18如以logv/Vm-v對log[S]作圖,也可得一直線(見下圖)。
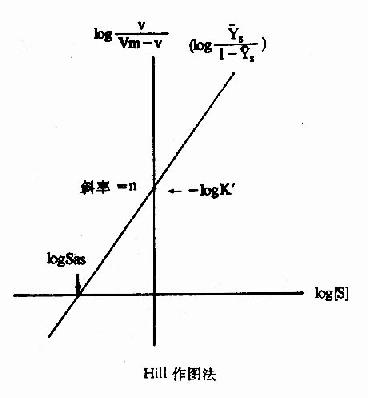
Hill作圖法
如v=Vm/2時,式6-19為log1=nlog[S]-logK'S=0(6-19)
此時的[S]即S0.5,故nlogS0.5=logK'5(6-20)式6-18所得的直線斜率為n,縱軸截距為-logk'S,而橫軸截距為logK'S/n,即log[S]0.5,但[S0.5]也可在已知logK'S后通過式6?0求取。
上節已述及,S0-5就相當于米曼氏動力學中的Km,當K0《k-1/k1時,可反映別構酶對底物的親和力,S0.5愈小,親和力愈大,而K's實際上已與親和力關系不大,因受到n的影響。故反映底物親和力的參數,已從非別構酶的Km一項移到別構酶的[S]一項,并且式6?0可看出K'S是隨[S]而改變的,不是一個常數。由于K'S的測定是假設V=(1/2)Vm或[S]=S0.5的條件下計算的,故有些作者用S0.5S,來代表別構酶的K'5,以免與Km混淆。